EL CICLO OTTO
El ciclo Otto fue estudiado por Beau de Rochas en 1862, siendo Otto quien lo aplicó en 1867 a un motor de gasolina. El fluido de trabajo es una mezcla de aire y gasolina finalmente pulverizada, que se combustiona en el volumen mínimo que esta sobre la cabeza de un pistón que se encuentra en su posición superior (PMS – punto muerto superior). Esta combustión es iniciada por una chispa de una bujía. El trabajo se produce cuando la mezcla de aire y gases de la combustión calientes se expande llevando el pistón a su posición inferior (PMI – punto muerto inferior). La relación del volumen cuando el pistón esta en el PMI al volumen cuando está en el PMS se denomina relación de compresión.
![]()
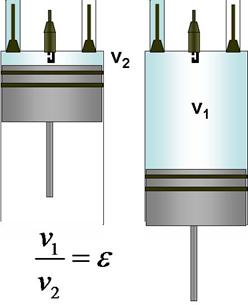
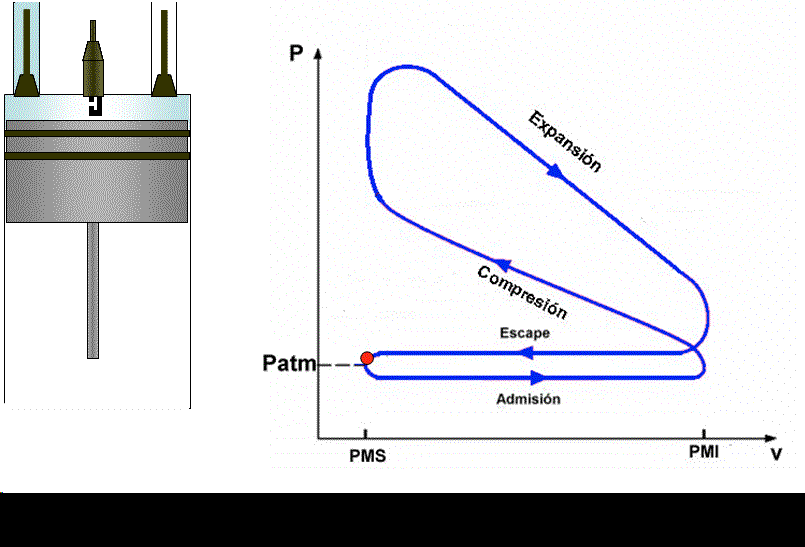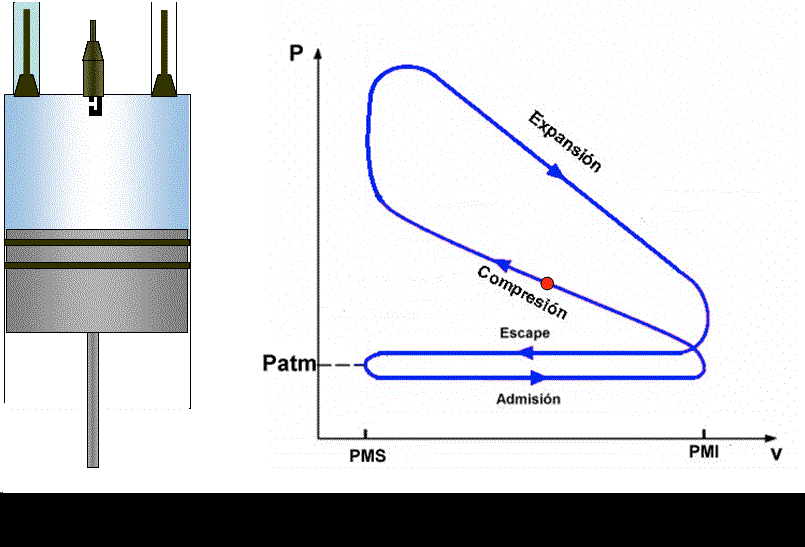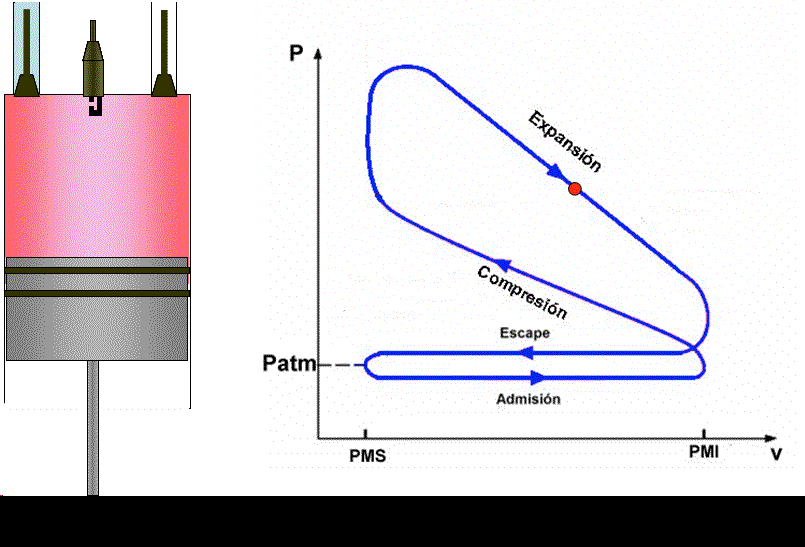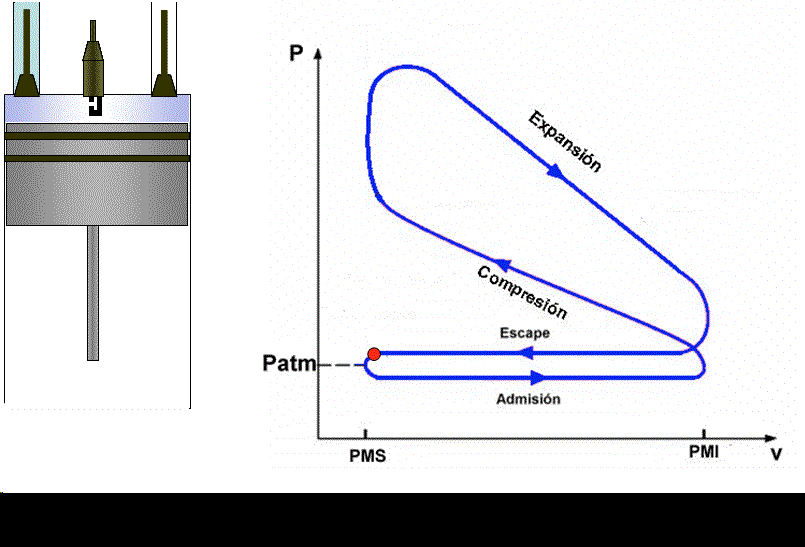
El ciclo se compone de dos transformaciones adiabáticas y dos isócoras y puede ser de 2 ó 4 tiempos. Para un motor de 4 tiempos, de acuerdo con la figura siguiente, se tiene:
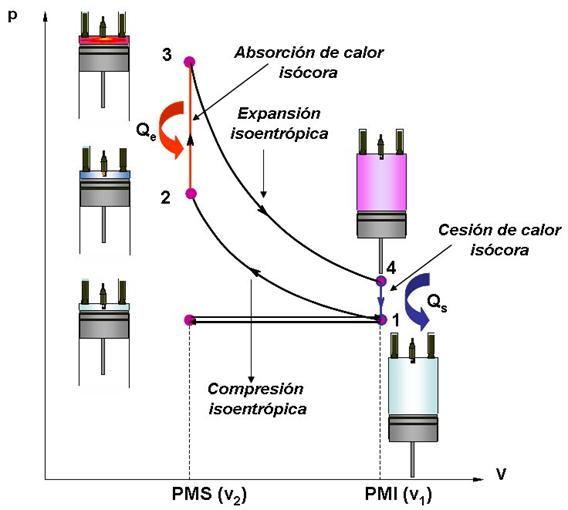
Primer tiempo (0 → 1): Se produce la admisión o aspiración de la mezcla aire – combustible a través de la válvula de admisión.
Segundo tiempo (1 → 2): Con las válvulas cerradas el émbolo recibe un trabajo que le permite realizar la compresión adiabática de la mezcla, al final de la cual el volumen de la mezcla (aire-combustible) se ha reducido al de la cámara de combustión aumentando la presión hasta un valor máximo que depende de la relación de compresión ε.
Tercer tiempo (2 → 4): Llegado el pistón al PMS salta una chispa, se combustióna la mezcla comprimida a una presión elevada y se efectúa la explosión (2 → 3) a volumen constante, aumentando la temperatura a, 1500ºC < T3 < 2200°C, y la presión a, 30 < p3 < 40 atm, recibiendo el fluido Qe (calor que entra), kiloJoules de la fuente caliente (que no es más que la liberación de la energía química de la mezcla que se combustiona. A continuación, el sistema constituido por los productos de la combustión realiza la expansión adiabática (3 → 4) hasta alcanzar el punto muerto inferior 4 que se corresponde con el volumen máximo V1, realizándose el trabajo.
Cuarto tiempo (4 → 0): Se abre la válvula de escape y se produce un descenso de presión (4 → 1) con el consiguiente enfriamiento isocórico en el cual se ceden Qs (calor que sale), kiloJoules a la fuente fría. A continuación el pistón avanza al PMS y expulsa los gases producto de la combustión(escape). Ya en el PMS se abre la válvula de admisión y se vuelve a introducir una nueva mezcla de aire y combustible en repitiéndose el ciclo.
En la práctica, para un ciclo real, la combustión teórica a volumen constante no se puede reali-zar, ni tampoco sería aconsejable hacerlo por el golpe brusco que ello significa y las cargas sobre los componentes del motor. Como el proceso real debe aproximarse al ideal, es necesario que se produzca el encendido antes de llegar el émbolo al punto muerto superior 3. Con este avance en el encendido se logra un mejor rendimiento.
Además, para tener bajas temperaturas en las superficies del pistón en contacto con la camisa del émbolo y lograr una buena lubricación disminuyendo el rozamiento, el cilindro va rodeado de un sistema de refrigeración; además, como las transformaciones (1 → 2) y (3 → 4) no son del todo adiabáticas no se llegan a alcanzar las temperaturas que corresponderían al ciclo ideal.
En el ciclo real, la admisión de la mezcla fresca se hace a una presión algo inferior a la atmosférica y el escape de los gases de la combustión a una presión algo superior. El ciclo se ve como sigue:
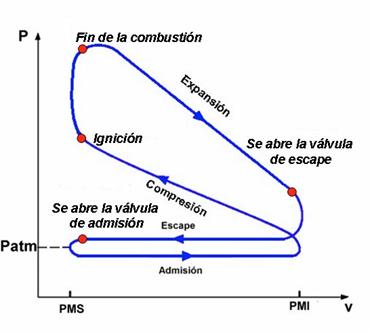
El diagrama T – S tien la forma siguiente:
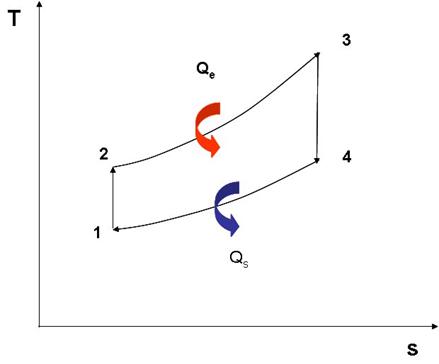
Una animación del ciclo se muestra a continuación:

Cálculo del rendimiento del ciclo Otto (Ver ejemplo resuelto).
Para el cálculo del rendimiento del ciclo teórico no se considera la masa de gasolina que se mezcla con el aire, pues es una fracción muy pequela del volumen de este último.
Partiendo de la definición de eficiencia y considerando que los calores evolcionan a volumen constante tendremos que:
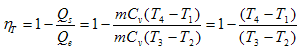
Como v3=v2 y v4=v1 para los procesos adiabáticos:
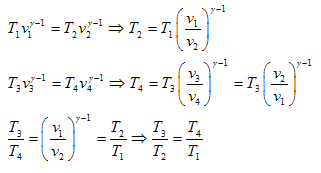
Entonces:
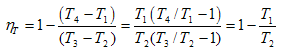
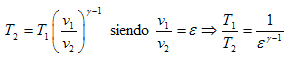
Lo que conduce finalmente a:
![]()
O sea que la eficiencia térmica teórica depende de la relación de compresión y del coeficiente adiabático γ llegándose a alcanzar rendimientos del orden del 40% al 54%. Pudiera pensarse que sería factible obtener mayores rendimientos aumentando el grado de compresión. Sin embargo esto se ve limitado por las características del combustible que se utiliza, que es la gasolina. En la gasolina se busca una buena evaporabilidad (para que la mezcla con el aire sea más eficiente). Esto implica la utilización de fracciones ligeras del petróleo. Las características de los hidrocarburos que las componen son tales, que su tendencia a la autoinflamación a elevadas temperaturas y presiones son elevadas. Esta autoinflamación se origina por los procesos de formación de hidroperóxidos y peróxidos por reacciones en cadena. Los hidrocarburos ramificados y los hidrocarburos aromáticos tienen una mayor resistencia a que ocurran estas reacciones. Los procesos de autoinflamación espontánea dan lugar a focos secundarios de ignición y a que se originen ondas de choque asociadas a los frentes de llama que se encuentran, digamos que no están previstas en el diseño. Esto da lugar al surgimiento de golpeteos en el motor en un proceso (debido a variaciones de la presión con respecto a la nominal para un ángulo f de giro del cigüeñal), que se denomina combustión detonante, como se ilustra a continuación:
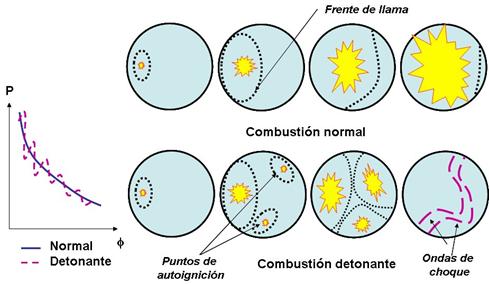
La resistencia de las gasolinas a la detonación se denomina estabilidad antidetonante y se mide por el npumero de octano u octanaje. El incrmento del grado de compresión motivó el incremento de las exigencias a la estabilidad antidetonante de las gasolinas. Esto se logró con la adición de aditivos como el tetraetilo de plomo. Sin embargo este producto es altamente contaminante, por lo que ha quedado prohibida su adición a las gasolinas. El incremento de la estabilidad antidetonante de las gasolinas se logra mediante el empleo de mezclas de fracciones con alto octanaje (de la reformación catalítica, etc.) y en la actualidad se utilizan mezclas con otros componentes como el etanol. En la práctica las relaciones de compresión van desde 6 ÷ 8 para gasolina de bajo octanaje y de 8 ÷10 para gasolina de alto octanaje, alcanzándose en el PMS en la compresión, presiones, de 12,3 ÷ 18,4 atm y de 18,4 ÷ 25 atm respectivamente.
Los rendimientos del ciclo real también resultan distintos al teórico porque en la realidad tenemos mezclas aire – combustible y aire – productos de la combustión cuyos CV son distintos a los del aire que son los que se utilizan en los cálculos.
08/11/2012