Cálculos de un ciclo Rankine ideal.
Para ilustrar la manera de abordar los cálculos del ciclo Rankine utilizaremos un ejemplo resuelto, enfatizando en la conveniencia de seguir los pasos para resolver problemas que ya fueron enunciados con anterioridad.
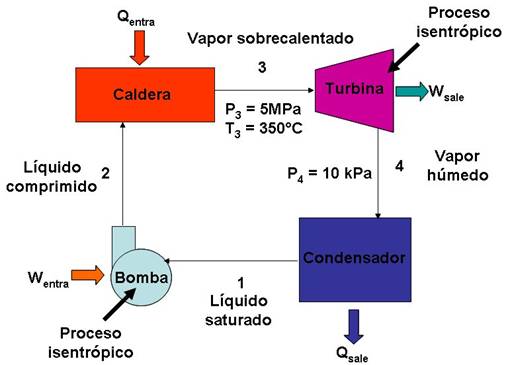
En un ciclo Rankine ideal, el vapor sale de la caldera a 5 Mpa y 350°C y es condensado a 10 kPa. Determine los valores de P, T, h y s en cada paso del ciclo, el trabajo neto producido y la eficiencia del ciclo.
Solución. El esquema del ciclo, considerando las características de los procesos en la turbina y la bomba, así como los estados, se muestra en la figura siguiente:

El primer paso es construir la tabla con los estados y las variables que nos piden o son necesarias.
|
|
Estado 1 |
Estado 2 |
Estado 3 |
Estado 4 |
|
Estado |
Liq. Saturado |
Liq. Comprimido |
Vap. Sobrecalentado |
Vap. Húmedo |
|
Presión, bar |
0.1 |
50 |
50 |
0.1 |
|
Temperatura, °C |
|
|
350 |
|
|
h, kj/kg |
|
|
|
|
|
s, kj/kg-K |
|
|
|
|
En negrita aparecen los datos que nos dan en el problema y lo que sabemos de los estados por las características del ciclo Rankine. Con las tablas de vapor o con algún programa adecuado (usaremos steamtab.exe), podemos calcular de inmediato las variables que aparecen a continuación subrayadas.
|
|
Estado 1 |
Estado 2 |
Estado 3 |
Estado 4 |
|
Estado |
Liq. Saturado |
Liq. Comprimido |
Vap. Sobrecalentado |
Vap. Húmedo |
|
Presión, bar |
0.1 |
50 |
50 |
0.1 |
|
Temperatura, °C |
45.8 |
45.8 |
350 |
45.8 |
|
h, kJ/kg |
191.806 |
|
3069.31 |
|
|
s, kJ/kg-K |
0.649196 |
0.649196 |
6.45157 |
6.45157 |
Nótese que s1 = s2 y s3 = s4 por ser procesos isentrópicos. Utilizando el valor de presión y entropía para el estado 2 podemos hallar la entalpía de este estado (196.842 kJ/kg). Con los datos de la entalpía del líquido saturado y la del vapor a 0.1 bar, podemos calcular la entalpía del estado 3 recordando que:
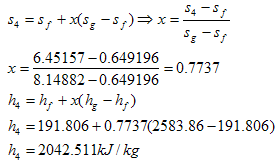
Y la tabla queda finalmente:
|
|
Estado 1 |
Estado 2 |
Estado 3 |
Estado 4 |
|
Estado |
Liq. Saturado |
Liq. Comprimido |
Vap. Sobrecalentado |
Vap. Húmedo |
|
Presión, bar |
0.1 |
50 |
50 |
0.1 |
|
Temperatura, °C |
45.8 |
45.8 |
350 |
45.8 |
|
h, kJ/kg |
191.806 |
196.842 |
3069.31 |
2042.511 |
|
s, kJ/kg-K |
0.649196 |
0.649196 |
6.45157 |
6.45157 |
Evidentemente del esquema vemos que:
Qentra = h3 – h2 = 3069.31 – 196.842 = 2872.47 kJ/kg
Wsale = h3 – h4 = 3069.31 – 2042.51 = 1026.8 kJ/kg
Qsale = – (h4 – h1 = – (2042.51 – 191.806) = – 1850.71 kJ/kg
Wentra = – (h2 – h1)= – (196.84 – 191.81) = – 5.03 kJ/kg
Por consiguiente el trabajo neto será:
Wneto = Wsale + Wentra = 1026,8 – 5.03 = 1021.8 kJ/kg
La eficiencia será:
h = Wneto/Qentra = 1021.8/2872.47 = 0.3557
Obteniéndose el mismo valor si utilizamos la ecuación h = 1 – Qsale/Qentra